Nat Commun|浙江大学转化医学研究院孙毅教授课题组发现Ube2m-Rbx1拟素化-泛素化轴维持调节性T细胞的功能特性
2022年5月31日,浙江大学医学院附属第二医院肿瘤研究所/浙江大学转化医学研究院孙毅教授团队在Nature Communications在线发表论文,发现Ube2m-Rbx1拟素化-泛素化轴维持调节性T细胞的功能特性。

Cullin-RING ligases(CRLs)是最大的泛素E3连接酶家族,介导约20%细胞内蛋白质的泛素化修饰1。不同成员的CRLs成员由不同的亚基组成,其催化亚基共有两种,分别是Rbx1/Roc1和Rbx2/Rnf7/Sag2。孙毅教授课题组前期工作发现,Rbx1或Sag在小鼠的胚胎发育过程中都起到至关重要的作用,无论是敲除敲除Rbx1还是Sag,都会导致小鼠胚胎期死亡,且小鼠胚胎存活时间和死因不同3,4,这表明Rbx1和Sag虽然序列和结构相近,但是并不是功能冗余的,而是具有功能的独立性。
调节性T细胞(Treg细胞)是一类重要的免疫抑制性细胞,对于维持机体免疫稳态,抑制免疫细胞过度活化发挥重要作用;转录因子Foxp3是Treg细胞重要的标志分子5。一些Foxp3以外的蛋白质也能够调控Treg细胞的功能。
孙毅教授带领课题组研究人员进一步利用Foxp3Cre-Loxp系统,交配产生Foxp3Cre;Rbx1fl/fl和Foxp3Cre;Sagfl/fl小鼠,在Treg细胞中分别敲除Rbx1和Sag基因。Foxp3Cre;Sagfl/fl小鼠没有明显的炎症反应,小鼠健康可育。Foxp3Cre;Rbx1fl/fl小鼠在出生后30天左右死亡,并出现严重的炎症反应。Treg细胞中敲除Rbx1引发的表型,与在小鼠中去除Treg细胞引发的表型5非常相似,表明Rbx1在Treg细胞中发挥至关重要的调控作用;同时Rbx1和Sag敲除的区别,也进一步验证了Rbx1和Sag功能上相对独立性。
虽然在Rbx1缺失的Treg细胞,在小鼠出生后逐渐降低;但是在刚刚出生8天的幼鼠体内,Treg细胞比例正常,同时免疫细胞的过度活化就已经很明显了,这表明Rbx1缺失导致Treg细胞免疫抑制功能缺失。
为了深入研究Rbx1对Treg细胞分化的影响,研究人员使用单细胞转录组测序技术,对野生型和Rbx1缺失的Treg细胞进行分析。通过单细胞转录组测序技术,小鼠Treg细胞可以被进一步分解为10余个亚群,其中的两个亚群在Rbx1缺失的Treg细胞中比例明显降低;而这两个亚群高表达多种Treg细胞的关键功能分子,是效应性Treg细胞亚群。Rbx1缺失导致Treg细胞中静稳亚群无法向效应亚群分化。
Rbx1是一种泛素E3连接酶,能够催化底物蛋白的泛素化,促进其降解。为了寻找Rbx1在Treg细胞中的底物蛋白,研究人员对Rbx1缺失的Treg细胞进行了质谱蛋白质组检测,分析到了大量蛋白质丰度的变化。结合转录组分析的结果,研究人员找到了57种蛋白质,在Rbx1缺失的Treg细胞中蛋白质丰度升高,且同时对应的mRNA水平基本不变。这57种蛋白很可能是Rbx1介导泛素化的直接底物,特别是其中一些蛋白质已经被证实能够被Rbx1催化发生泛素化修饰,更证明了本策略是可靠的。
在这57种潜在的Rbx1直接底物中,Bim蛋白也被证实可被Rbx1泛素化并降解,同时Bim与细胞凋亡6和Treg细胞7都有一定关联,因此猜测Bim的积累,很可能部分介导了Treg细胞中Rbx1缺失引发的表型。在Treg细胞中同时敲除Rbx1和Bim,小鼠仍然发生炎症反应,但是强度较单独敲除Rbx1的小鼠要弱一些。表型挽救实验证实Bim确实部分参与了Rbx1在Treg细胞中的功能。
蛋白质拟素化是一种类泛素化修饰,由类似于泛素化的E1-E2-E3酶促级联反应催化完成;拟素化修饰对于CRLs的活性非常重要,其中拟素化E2耦联酶Ube2m是Rbx1的上游,拟素化E2耦联酶Ube2f是Sag的上游8。在Treg细胞中敲除Ube2f,小鼠没有明显的炎症反应,和敲除Sag相似。令人惊奇的是,在Treg细胞中敲除Ube2m,引发的表型要远远弱于Rbx1缺失引发的,表明在Treg细胞中,Rbx1的功能只是部分依赖于Ube2m,与经典观点不同,暗示了Ube2m-Rbx1调控的复杂性。
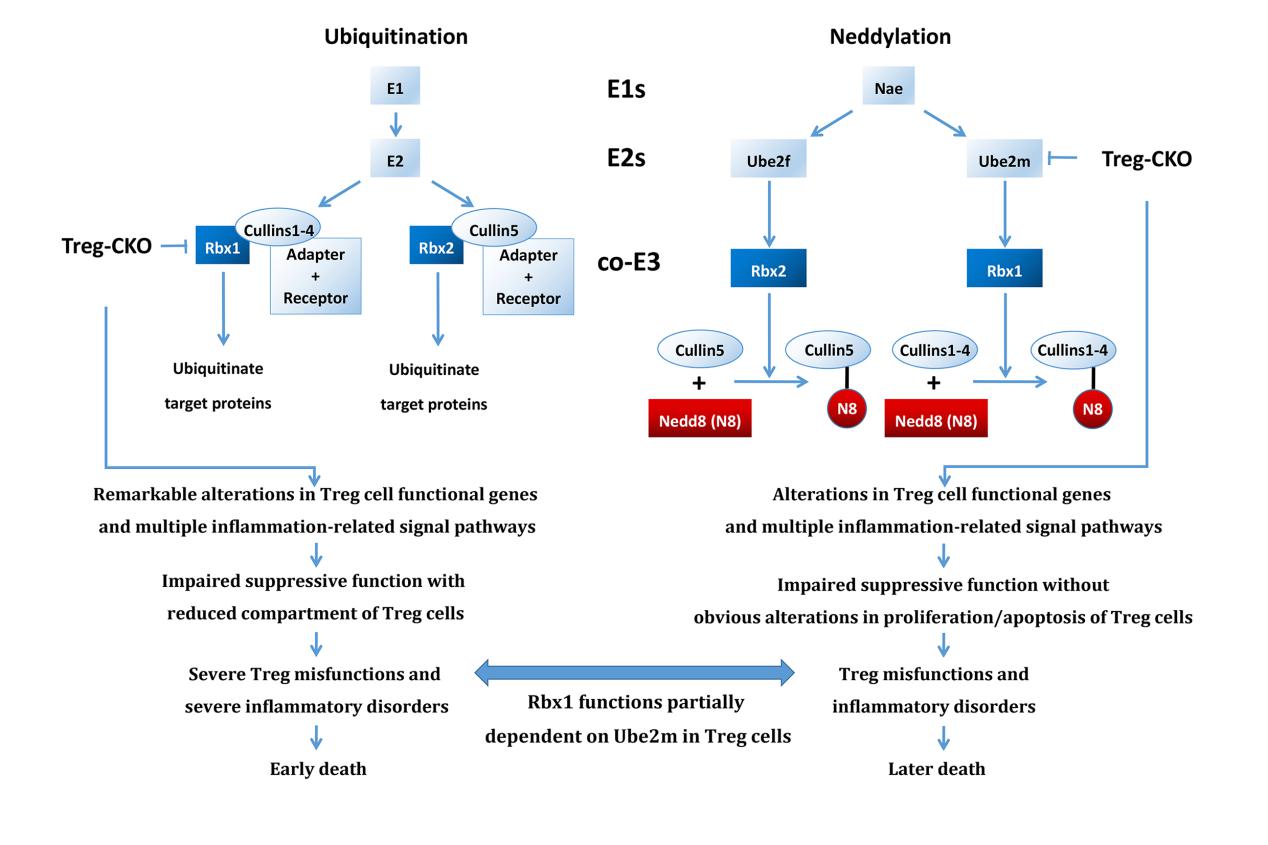
图1 Rbx1和Ube2m在Treg细胞功能调节中的工作模型
浙江大学医学院附属第二医院肿瘤研究所吴迪是本文第一作者,孙毅教授是本文通讯作者。本项目蛋白质质谱研究由国家蛋白质科学中心(北京)秦钧教授课题组开展。项目得到了国家重大研究计划、国家自然科学基金和浙江省自然科学基金的支持。
参考文献:
Soucy, T. A. et al. An inhibitor of NEDD8-activating enzyme as a new approach to treat cancer. Nature458, 732-736 (2009).
2. Zhao, Y. & Sun, Y. Cullin-RING ligases as attractive anti-cancer targets. Curr. Pharm. Des. 19, 3215-3225 (2013).
3. Tan, M., Davis, S. W., Saunders, T. L., Zhu, Y. & Sun, Y. RBX1/ROC1 disruption results in early embryonic lethality due to proliferation failure, partially rescued by simultaneous loss of p27. Proc. Natl. Acad. Sci. U. S. A. 106, 6203-6208 (2009).
4. Tan, M. et al. SAG/RBX2/ROC2 E3 ubiquitin ligase is essential for vascular and neural development by targeting NF1 for degradation. Dev. Cell 21, 1062-1076 (2011).
5. Kim, J. M., Rasmussen, J.P. & Rudensky, A.Y. Regulatory T cells prevent catastrophic autoimmunity throughout the life span of mice. Nat. Immunol.8, 191-197 (2007).
6. O'Connor, L., et al. Bim: a novel member of the Bcl-2 family that promotes apoptosis. EMBO J. 17, 384-395 (1998).
7. Chougnet, C. A. et al. A major role for Bim in regulatory T cell homeostasis. J. Immunol. 186, 156–163 (2011).
8. Huang, D. T. et al. E2-RING expansion of the NEDD8 cascade confers specificity to Cullin modification. Mol. Cell33, 483-495 (2009).


