杨巍/余沛霖团队揭示纳米材料引发肺部炎症反应的分子机制
随着科学技术的日新月异,纳米材料已经广泛应用于日常生产生活中的各行各业,包括化妆品、食品、药品等领域,人群暴露风险也随之持续增加,因此,纳米材料的安全性也越来越受到关注。作为最主要的暴露方式之一,已有研究发现纳米颗粒经呼吸道暴露后可以引起严重的肺部损伤,临床上已有职业工人由于纳米材料持续暴露引发胸膜积液、肺间质性炎症和肺纤维化、并最终导致死亡的案例报道。尽管有研究提示,氧化应激在纳米颗粒物引发炎症的过程中起着关键作用,但具体分子机制尚不清楚。
TRPM2(Transient Receptor Potential Melastatin 2,TRPM2)是一种非选择性阳离子通道,在体内广泛表达,包括脑、骨组织、肝脏、血液、免疫系统等。近年来的大量研究报道, TRPM2作为一种氧化应激感受器,在脑卒中、阿尔茨海默症、糖尿病、脓毒症以及多种肿瘤疾病的发生发展和转归中发挥重要作用。该通道的内源性激动剂是腺苷二磷酸核糖ADPR,它是一种聚腺苷二磷酸核糖聚合酶(Poly(ADP-ribose) polymerase-1,PARP-1)通过催化多种核蛋白进行多聚腺苷二磷酸核糖基化而生成的核苷类似物。已知氧化应激是胞内引发DNA 损伤最重要的分子事件之一,过量生成的活性氧(reactive oxygen species,ROS)将造成DNA链断裂后引起PARP-1活化,从而通过增加ADPR的合成激活TRPM2通道。
近日,浙江大学医学院杨巍/余沛霖课题组在国际著名毒理学期刊Particle and Fibre Toxicology(5年影响因子:8.40)上发表了题为Silica nanoparticles induce lung inflammation in mice via ROS/PARP/TRPM2 signaling-mediated lysosome impairment and autophagy dysfunction的研究论文,揭示了纳米二氧化硅颗粒(silica nanoparticles,SiNPs)通过ROS/PARP-1/TRPM2信号通路引发肺部炎症的分子机制,为揭示纳米材料介导的肺部损伤机制提供了新的视角,同时为纳米材料引发的炎症性疾病的预防和治疗提供了新的靶点。

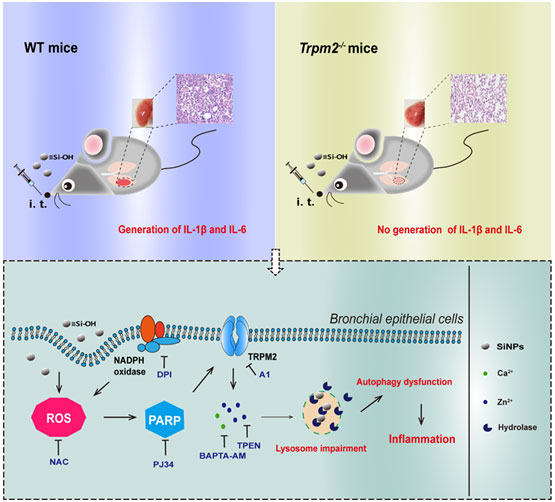
在本研究中,研究者通过支气管灌注C57BL/6野生型(WT)小鼠构建了SiNPs引发肺部炎症的动物模型,发现暴露组小鼠支气管肺泡灌洗液中的细胞因子水平、蛋白浓度、乳酸脱氢酶释放和炎性细胞浸润均显著升高,证实SiNPs暴露引发小鼠肺部炎症。已知肺支气管上皮细胞是纳米材料肺损伤的首要接触细胞,为此,研究者使用人支气管上皮细胞观察了SiNPs 的体外毒性效应,发现经SiNPs 暴露后细胞活力明显下降,炎症水平则明显升高,这一结果与体内结果一致。进一步的研究发现,SiNPs 可以引起细胞内ROS生成明显增加,进而激活PARP-1产生TRPM2通道激动剂ADPR,并引发TRPM2 通道开放介导胞内Zn2+和Ca2+水平的升高,由它们协同导致溶酶体碱化和溶酶体膜通透性改变,破环溶酶体功能,进而阻断正常细胞自噬过程并引发炎症反应。最后,研究发现SiNPs灌肺处理后,TRPM2敲除小鼠的肺部炎症水平显著低于野生型小鼠,而且TRPM2敲除小鼠的肺损伤也显著减轻,从而在动物水平进一步表明ROS/PARP-1/TRPM2信号通路在SiNPs引发的肺部炎症过程中发挥的重要功能。
浙江大学公共卫生学院硕士生王铭祥和李金博士为本文的共同第一作者,浙江大学公共卫生学院余沛霖副教授、基础医学院杨巍教授和浙江大学高分子科学与工程学系杜滨阳教授为本文的共同通讯作者。
原文链接:https://particleandfibretoxicology.biomedcentral.com/articles/10.1186/s12989-020-00353-3


