浙江大学药学院高建青教授团队构建氧化铁纳米粒增强的干细胞载体系统实现对脑胶质瘤的高效靶向自杀基因治疗
针对肿瘤组织的自杀基因治疗在提高药物对肿瘤细胞的选择性,减少化疗药物的毒副作用等方面具有独特的优势。近年来的研究也显示自杀基因疗法在恶性脑胶质瘤的治疗中具有巨大的应用潜力。然而,这一治疗系统在实际应用中也面临着一些不足和挑战,比如如何实现自杀基因在脑部胶质瘤组织的高效表达;以及如何克服胶质瘤细胞因为低表达的细胞间隙连接蛋白43(Connexin 43,Cx43)而对自杀基因的旁观者杀伤效应的敏感性不足。上述这些问题对进一步提高自杀基因疗法用于脑胶质瘤治疗的有效性和安全性提出了挑战。针对这一挑战,我院高建青教授团队研发成功了一种基于氧化铁纳米粒增强的间充质干细胞(Mesenchymal stem cells,MSCs)载体系统。通过该细胞载体系统不但实现了自杀基因向脑胶质瘤组织的高效靶向递送,还能通过氧化铁纳米粒上调的Cx43蛋白表达显著提高胶质瘤细胞对旁观者杀伤效应的敏感性,最终实现良好的抑瘤效果。相关研究发表于生物医学1区杂志《Theranostics》(2021 IF: 11.556)。

MSCs是人体内一类存在于脂肪、骨髓和脐带血等的成体干细胞,其具有天然的穿透血脑屏障以及向肿瘤组织进行归巢的特性。因此,可以成为一种良好的脑部肿瘤靶向的细胞传递载体。但是,MSCs也存在对基因药物携载效率低,以及与胶质瘤细胞间的间隙连接通讯能力较弱(Gap Junction Intercellular Communication, GJIC)等问题,限制了旁观者效应杀伤作用的有效发挥。
在此项研究中,研究人员通过氧化铁纳米粒携载自杀基因对MSCs载体进行改良,最终实现了MSCs载体对自杀基因(Herpes simplex virus thymidine kinase,HSV-tk)的高效携载和向胶质瘤组织的靶向递送。研究还进一步发现,氧化铁纳米粒能上调MSCs的Cx43蛋白表达,并可以进一步影响与MSCs接触的胶质瘤细胞上的Cx43蛋白表达,从而显著促进MSCs与胶质瘤细胞间的GJIC的形成,为发挥旁观者效应的高效杀伤作用提供了重要的保障。通过该氧化铁纳米粒增强的MSCs载体相比未增强的MSCs载体明显促进了胶质瘤细胞的凋亡,显著抑制了脑胶质瘤的发展,延长了模型大鼠的生存期。
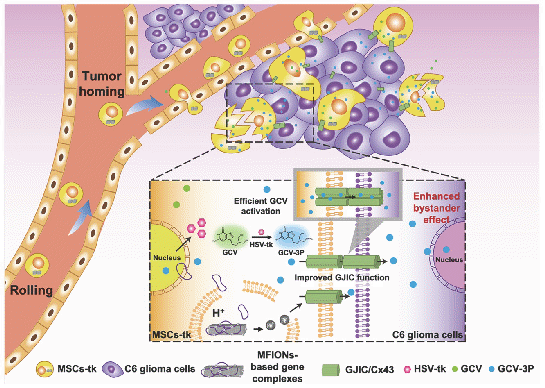
该研究利用氧化铁纳米粒同时实现了干细胞载体对基因药物的高效携载和与Cx43低表达的胶质瘤细胞间的GJIC形成,为进一步促进自杀基因疗法用于胶质瘤高效和安全的靶向治疗提供了新的思路。
我院的高建青教授为本文的通讯作者,课题组成员硕士研究生李艾和副研究员张添源博士为本文的共同第一作者。
原文链接:https://www.thno.org/v11p8254.htm


