转化医学研究院周民团队Advanced Science发文报道拉曼影像技术用于微小肿瘤灶检测及术后辅助治疗
发展高、精、尖的诊断技术,实现疾病的早期诊断并对治疗效果进行监测是现代医学领域的大力发展方向之一。随着医学影像的飞速发展,成像技术已经从解决“看得到”“看得清”等问题逐渐向“看的早”“看的准”“看的全”的方向发展,随着分子影像概念的提出,分子影像学也应运而生。随着国民健康意识的提高,实现“看的早”“看的准”“看的全”的同时,选择对自身无损伤的安全成像方式也是未来发展的大势所趋。表面增强拉曼(SERS)成像技术具有灵敏度高、背景干扰小、检测过程对样品无损伤等特点,并且拉曼探针具有特定的指纹图谱(高特异性)和超低信号干扰等优势,其在生物医学领域表现出巨大的应用前景。由于其应用环境特殊,当前研究多用于体外肿瘤诊断,在活体状态下多局限于脑胶质瘤等肿瘤的诊断和治疗。
近日,转化医学研究院周民团队在表面增强拉曼成像技术用于腹腔肿瘤精准诊疗应用方面取得新进展,在Advanced Science在线发表题为“Intraoperative Assessment and Photothermal Ablation of the Tumor Margins Using Gold Nanoparticles”的研究论文。
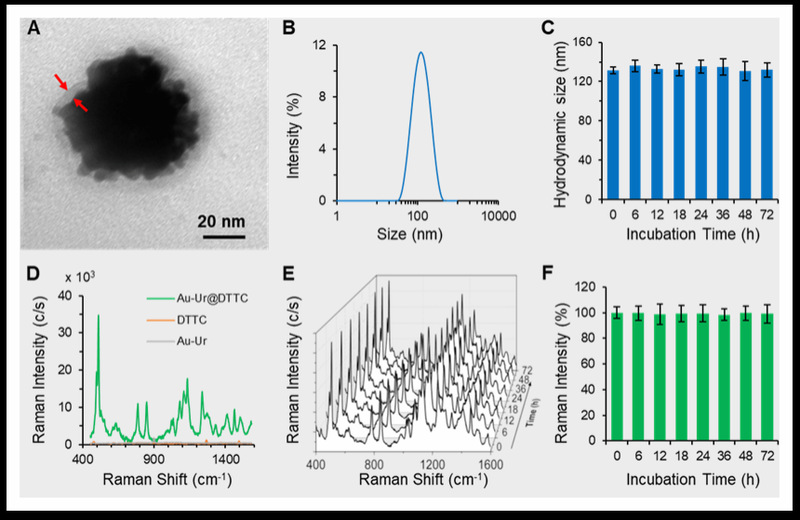
热点增强效应的表面增强拉曼影像探针具有高灵敏度及超强稳定性
肿瘤是世界范围内高发病率与死亡率的疾病。结肠癌和卵巢癌等腹腔肿瘤具有广泛的腹腔播散和转移特性,是恶性程度较高的肿瘤类型之一。由于这类恶性肿瘤通常具有较高的侵袭性和转移性,并且会浸润性迁移到周围组织和关键器官,临床上难以通过外科手术进行精准切除,导致较高的复发率、死亡率。本研究基于纳米金制备得到具有表面增强拉曼效应的纳米诊疗一体化拉曼探针,该探针表面布满海胆状毛刺结构,并接入拉曼报告分子(DTTC,一种近红外染料)。在近红外激光照射下该探针产生的灵敏度高、特异性强的拉曼信号可实现微小肿瘤灶的精准检测,并可用于拉曼影像介导下肿瘤的手术切除。同时,该探针具有良好的光热转换性能,在近红外激光照射时可产生光热治疗的效果,利用光热治疗作用实现对微小肿瘤灶的术后进一步清扫。综上,本研究构建了一种具有高灵敏度诊断功能并兼具光热性能的诊疗一体化纳米探针,并结合新型拉曼影像技术,实现了腹腔肿瘤的精准切除和术后清扫。研究揭示了拉曼影像技术在生物医学领域的应用潜力,并为转移性肿瘤的诊断和治疗提供了新策略。
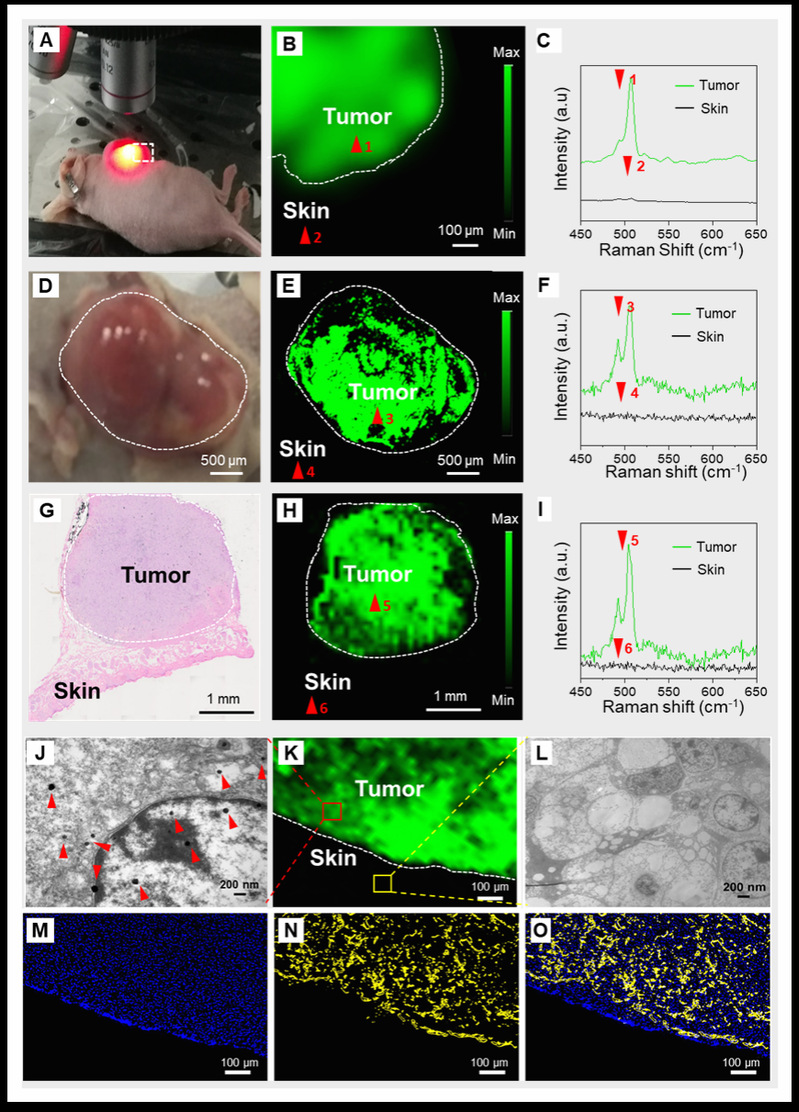
以纳米金为探针的拉曼影像技术可以清楚检测肿瘤边界
对于外科医生而言,尽管外科手术技术不断发展,但发展准确诊断并完全消除微小肿瘤的手术技术仍然是一个巨大的挑战。目前的临床策略主要依赖于成像技术,如正电子发射断层扫描(PET)和磁共振成像(MRI),可实现对术前肿瘤位置的确定。然而,由于手术期间组织移位,肿瘤的术前图像通常与实际位置不一致,导致肿瘤切除不够准确而无法在术中诊断和消除微小残留肿瘤,仍是癌症手术中面对的一大难题。这些残留的微小肿瘤灶通常是引起致死性复发和转移的主要原因,寻找更精准的术中肿瘤成像技术和成像技术引导下的手术切除成为现阶段研究的热点和重点。随着光学显微成像技术的发展,在光学探针的帮助下,利用荧光成像技术检测肿瘤生物标志物是肿瘤早期诊断的重要策略,荧光显微成像作为最常用的成像手段已经获得了长足的发展。但荧光成像需要的荧光基团通常存在光漂白、光损伤、组织穿透深度差等问题。拉曼影像技术作为一种强大的无损伤成像技术,可以有效弥补上述成像技术的不足。
目前,针对具有转移特性的腹腔肿瘤临床上常规治疗方法主要是手术切除联合腹腔灌注热化疗技术。手术切除过程中需要对肿瘤边界进行尽可能精确的确定,准确诊断并完全消除微小肿瘤仍然是一个巨大的挑战。对于一些生长过程中会浸润到周围重要器官或神经结构的肿瘤,经验丰富的外科医生也难以通过手术彻底切除以致微小肿瘤灶残余,进而发生致命性的肿瘤复发和转移而影响预后情况。表面增强拉曼成像技术具有很高的灵敏度和特异性,可以实现对多种物质的检测,本研究设计构建的拉曼探针,具有较好的生物相容性,能够在肿瘤部位滞留足够长的时间;拉曼信号强,单次注射即可实现术前和术中成像,实现肿瘤边缘的精准确定并介导肿瘤的手术切除。虽然腹腔灌注热化疗可以改善患者预后,但这种非特异性的辅助治疗方式同时会损害其它健康器官并引起并发症。因此,对肿瘤边界进行精准的诊断提高医生的手术切除率,同时在无副作用的情况下利用特异性的光热治疗作用根除残余的微小肿瘤灶,是改善病人术后的复发情况和生存率的重要研究方向,对播散性腹腔肿瘤的治疗和未来肿瘤诊断治疗领域的发展至关重要。
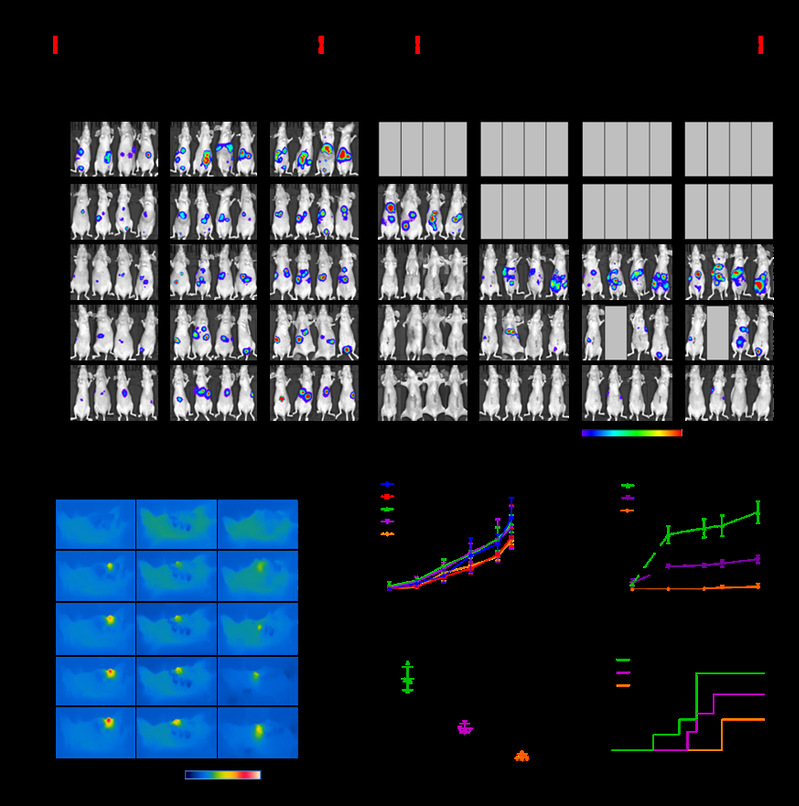
拉曼影像技术实现术后辅助光热治疗,改善肿瘤复发状况
该研究成果是该团队基于拉曼成像技术的纳米诊疗一体化在生物医学应用领域的又一创新性突破。同时,该团队还开展了基于表面增强拉曼探针的拉曼成像技术监控下的耐药菌感染伤口灭菌及促愈合研究(Biomaterials,2020),可实现伤口上残留的细菌的实时精确的影像监控,为临床医生掌握治疗的黄金时期提供更加有效的途径。团队并受邀在国际期刊发表多篇拉曼影像领域综述论文(WIREs Nanomedicine & Nanobiotechnology,2021)(Acta Pharmaceutica Sinica B,2018)。该研究工作得到了浙江大学恶性肿瘤预警与干预教育部重点实验室、现代光学仪器国家重点实验室的大力支持和国家重点研发计划、国家自然科学基金、中央军委科技委等项目资助。
浙江大学转化医学研究院交叉学科博士生魏巧琳(时任杭州师范大学医学部特聘副教授)为本文的第一作者,浙江大学转化医学研究院博士后李杨杨等为本文的共同第一作者,周民研究员为论文唯一通讯作者。
论文链接:http://dx.doi.org/10.1002/advs.202002788


