转化医学院周民团队《Biomaterials》发文:可规模化生产低毒氧化铪纳米药物用于增强肿瘤放射治疗
2019年10月11日,浙江大学医学院转化医学研究院周民研究员团队在生物材料领域顶级期刊《Biomaterials》(IF=10.273)在线发表题为“Gram-scale synthesis of highly biocompatible and intravenous injectable hafnium oxide nanocrystal with enhanced radiotherapy efficacy for cancer theranostic”的研究论文。该成果核心内容是设计构建可大量合成、具有高生物相容性和可用于静脉注射的氧化铪纳米药物,用于肿瘤放疗增敏治疗。
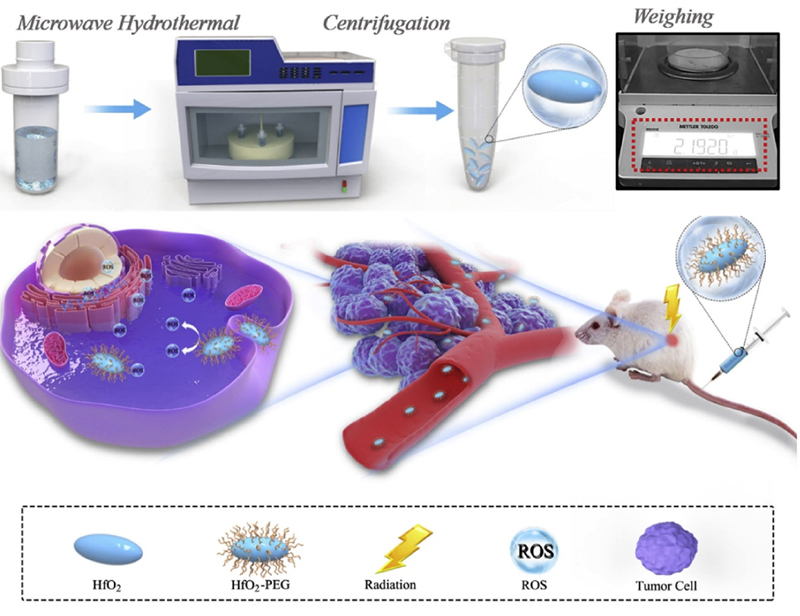
生物无机纳米材料是当前生物材料研究热点,然而能成功应用于临床试验的仅有有限的几种材料。以氧化铪(HfO2)为基础的NBTXR3纳米肿瘤放射治疗增敏剂已于近年来成功开展临床试验研究,是目前应用于临床试验的为数不多的无机纳米材料之一。但是,目前临床上报道的应用于放疗增敏的HfO2是主要依赖于肿瘤内注射的方式,极大的限制了可治疗的肿瘤类型及治疗效果。为了克服这一限制,在这项工作中,周民团队开发了一种可大规模生产、静脉注射的新型HfO2纳米晶组装体,不但具有显著增强肿瘤放射治疗效果,而且可以从体内有效清除,减小其副作用。
现有的结果表明,该新型HfO2放疗增敏剂在X射线照射下不但可以高效地摧毁乳腺癌肿瘤细胞,同时还可以显著抑制肿瘤干细胞的生长。通过静脉注射后,CT以及活体荧光成像表明其高效的肿瘤部位富集的能力,并在4T1乳腺癌肿瘤模型中展现出高效的放疗增敏效果。更为重要的是,该氧化铪纳米放疗增敏剂即使在高浓度下,细胞以及体内的毒性都较低,而且可以在体内合理的时间内被有效的降解和排泄,避免长期的毒性。具有较高的临床转化前景。通过该新型放疗增敏剂,周民团队已经找到了一种能够提升肿瘤放疗治疗效率和治疗安全性的新方法。目前该研究仅限于小动物水平的验证,期待在大动物水平的实验验证工作,从而验证其转化的可行性。
论文的第一作者是浙江大学转化医学研究院/医学院附属第二医院博士后李杨杨,交叉学科博士生祁宇宸为论文共同第一作者,浙江大学转化医学院周民研究员是论文的唯一通讯作者。相关研究也得到了浙江大学交叉学科项目、国家重点研发计划、国家自然科学基金、浙江大学现代光学仪器国家重点实验室基金、中国博士后科学基金等项目的大力支持。

这是周民团队今年在《Biomaterials》期刊连续发表的第二篇关于肿瘤放射治疗的研究论文。前一篇文章是采用磁共振影像引导下肿瘤热疗增强放射治疗协同治疗研究。
论文链接:https://doi.org/10.1016/j.biomaterials.2019.119538
https://doi.org/10.1016/j.biomaterials.2019.119369


