郑树森院士团队在《HEPATOLOGY》发文揭示肝癌抗PD-L1治疗抵抗新机制
近日,浙江大学医学院附属第一医院郑树森院士团队在肝脏病领域著名学术期刊《HEPATOLOGY》(IF=14.09)上发表题为“Blocking TREM-1+ Tumor-associated macrophages induced by hypoxia reverses immunosuppression and anti-PD-L1 resistance in liver cancer” (缺氧微环境调控TREM-1+TAMs促进肝癌免疫抑制与抗PD-L1治疗抵抗)的研究论文。该论文发现肝癌缺氧微环境诱导的TREM-1阳性肿瘤相关巨噬细胞(TREM-1+TAMs)是造成肝癌抗PD-L1免疫治疗抵抗的主要原因,阻断TREM-1+TAMs为肝癌对抗PD-L1治疗的高效应答提供可能。

我国拥有全球最高的肝癌发病率。对于早期肝癌患者,手术切除是最佳治疗方案,但大部分患者就诊时已是肝癌晚期并失去手术机会。由于目前靶向药物索拉非尼(Sorafenib)与瑞格非尼(Regorafenib)的局限性,以抗PD-1/PD-L1轴为代表的免疫 “刹车点”药物为肝癌晚期患者提供了潜在的治疗手段。目前FDA批准针对PD-L1/PD-1轴的药物Opdivo (Nivolumab)于2018年6月进入中国,并在多种肿瘤治疗中取得了良好的效果。但是肝癌具有丰富的免疫抑制性细胞浸润特征,抗PD-1/PD-L1的治疗效果不佳;临床前期研究显示,肝癌对抗PD-1/PD-L1治疗应答率仅为14.3%。因此,改变肝癌抗PD-1/PD-L1治疗的无应答状态,探索新型的抗肝癌策略,改善患者预后是肝癌治疗的当务之急。
在本次研究中,郑树森院士团队首次阐明肝癌缺氧微环境是造成肝癌抗PD-L1治疗抵抗的始动因素。缺氧微环境作为实体瘤的普遍特征,特别在肝癌中,具有诱导肝癌耐药,血管生成,基质重塑等作用;但肿瘤相关免疫细胞特别是肿瘤相关巨噬细胞(TAMs)是如何对缺氧做出反馈尚不清楚。该研究发现在缺氧微环境中HIF-1α入核,通过结合TREM-1启动子上游-936~-929区域能显著上调TREM-1分子转录水平。此外TREM-1+TAMs与肿瘤缺氧程度密切相关,TREM-1+TAMs的高度富集提示肝癌进展与不良预后。通过模拟肝癌缺氧微环境和建立小鼠原位肝癌模型阐明:肝癌缺氧微环境中TREM-1+TAMs通过TREM-1/ERK/NF-κβ/CCL20信号通路招募的CCR6+Tregs是发挥免疫抑制和PD-L1抵抗的中心环节,这为多数肝癌患者不能受益于抗PD-1/PD-L1免疫治疗的内在原因提供了理论基础和潜在的解决方案。该研究通过设计TREM-1特异性非配体依赖型小分子多肽GF9(GLLSKSLVF),阻断CCR6+Tregs的趋化达到消除抗PD-L1治疗抵抗的效应,显著提高抗PD-1/PD-L1治疗在肝癌中的抗肿瘤效应,具有较好的临床转化前景。
该研究郑树森院士作为论文的通讯作者,吴秦川硕士研究生为第一作者。上述研究得到国家自然科学基金委重点项目、创新群体项目等的资助。
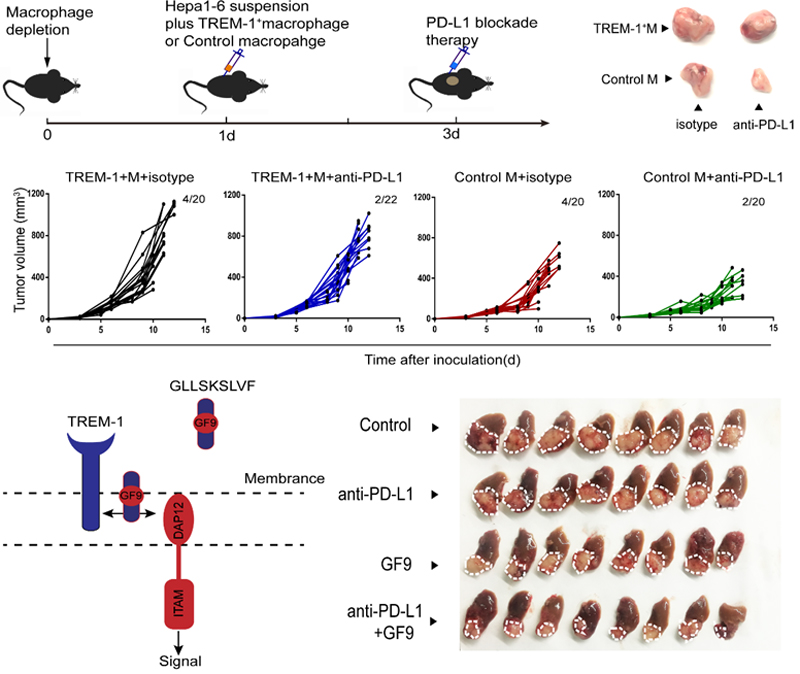
论文链接:https://aasldpubs.onlinelibrary.wiley.com/doi/abs/10.1002/hep.30593


