附属第一医院郑树森课题组发现超稳定纳米制剂能够有效根除肝癌
近日,医学院附属第一医院郑树森团队在国际著名学术期刊《Theranostics》(IF=8.766)上发表题为“Polylactide-tethered prodrugs in polymeric nanoparticles as reliable nanomedicines for the efficient eradication of patient-derived hepatocellular carcinoma”的研究论文。该论文报道了超稳定的7-乙基-10-羟基喜树碱(SN38)纳米制剂在人源的肝癌移植瘤模型中实现肿瘤的有效根除,为临床肝癌的化疗提供了可能的治疗手段。
我国是世界上最大的病毒型肝炎感染国,由此引发的肝癌发病率全球最高,其中半数以上肝癌发生在我国。对于早期肝癌患者而言,手术治疗是最佳方案,然而早期肝癌缺乏特异性症状,大部分患者就诊时已是肝癌晚期。对于这部分患者而言,往往采用药物姑息治疗。目前被FDA批准用于治疗晚期肝癌的药物仅有索拉非尼(Sorafenib)与瑞格非尼(Regorafenib),然而临床数据显示,索拉非尼在晚期肝癌病人中仅仅延长了2.8个月的中位生存期。因此,研发新型的抗肝癌策略是肝癌治疗的当务之急。
在癌症治疗领域,纳米药物及其制剂的临床应用取得了一定进展,其功效已在各种培养细胞系的移植瘤(cell-derived xenograft, CDX)动物模型中被证明有效。然而,在CDX动物模型上证明有效的纳米制剂在临床上的治疗效果并不尽如人意,这可能是因为CDX模型无法真实模拟肿瘤生物学行为和肿瘤微环境的一些特征。近年来,随着个体化精准医疗概念的提出,人源肿瘤异种移植瘤(patient-derived xenograft, PDX)模型在药物筛选和治疗研究的动物模型中更胜一筹。PDX模型是指将患者的肿瘤组织移植于免疫缺陷小鼠建立的异种移植模型,该模型由于较好地保留了原发肿瘤的遗传特性和异质性。
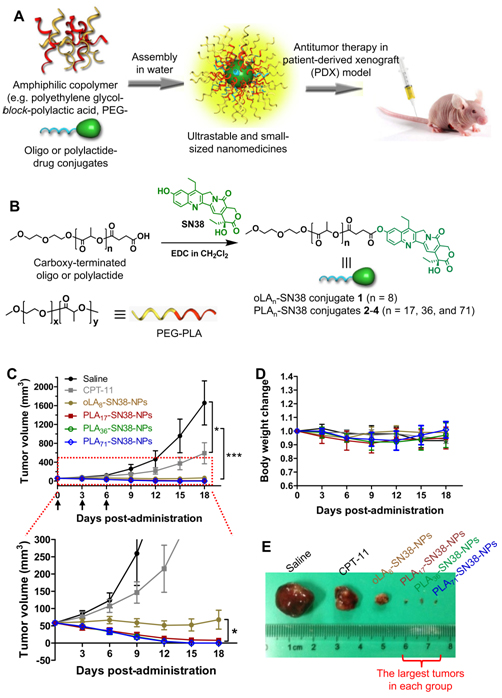
在本项研究中,郑树森团队基于前期发展的前药设计理念(Angew. Chem. Int. Ed., 2014, 53, 11532; Adv. Funct. Mater., 2015, 25, 4956; Cancer Res., 2017, 77, 6963),设计了第二代喜树碱衍生物SN38的前药。研究人员首先使用分子量不同的寡聚或高聚(oligo或poly)乳酸片段将SN38药物分子进行化学衍生,得到一系列SN38聚乳酸缀合物,发现所得前药能够与聚乙二醇-聚乳酸组装形成可系统注射的超稳定纳米胶束。相比短链聚乳酸修饰的SN38前药,长链聚乳酸修饰的药物在纳米胶束里面具有更好的缓释效果。此外,随着修饰的聚乳酸链长的增加,SN38药物的体内循环时间能有效延长。负载SN38的长循环纳米制剂在肝癌Hep 3B移植瘤模型中表现出优异的抗癌活性,经3次静脉注射给药后显示超过半数的肿瘤被消除。该药物在肝癌PDX小鼠模型中同样表现优异,7只裸鼠模型中,其中有5只的肿瘤被完全根除。更有趣的是,全身递送的纳米药物显著缓解了原药导致的血性腹泻。本项研究所使用的纳米药物载体为FDA批准的生物相容性较高的材料,具有较好的临床转化前景。
郑树森院士为论文的通讯作者,王杭祥副研究员为第一兼通讯作者。上述研究得到了国家自然科学基金委面上项目及创新群体项目等的资助。
参考文献:Polylactide-tethered prodrugs in polymeric nanoparticles as reliable nanomedicines for the efficient eradication of patient-derived hepatocellular carcinoma. Theranostics 2018;8(14):3949-3963.
原文链接:http://www.thno.org/v08p3949.htm


